Introduksjon
Den pediatriske intensivpasienten blir nøye monitorert med invasive måleinstrumenter, og barnet trenger tilfredsstillende sedasjon og smertelindring for ikke å fjerne nødvendig utstyr som tuber og katetre (1). Langvarig tilførsel av benzodiazepiner og/eller opioider øker imidlertid faren for medikamenttoleranse, deliriumutvikling og abstinens (2). Iatrogen abstinens (IA) betegner en tilstand som oppstår som følge av at man brått avslutter langvarig sedasjon og analgesi eller trapper ned legemiddeltilførselen for raskt (3). IA ses ofte i sammenheng med nedtrapping av benzodiazepiner og/eller opioider (4). I prospektive studier rapporteres det om en forekomst av IA hos barn som mottar disse legemidlene på 37–77 prosent ved bruk av kartleggingsverktøyet WAT-1 og 18–100 prosent ved bruk av kartleggingsverktøyet SOS (3,5). En nylig publisert norsk studie fant en prevalens for IA på 95 prosent ved bruk av WAT-1 (6). Risiko for utvikling av IA blir påvirket av behandlingslengde og dosering av opioider og/eller benzodiazepiner (7). En systematisk oversikt angir en insidens på 50 prosent hos barn som får kontinuerlig infusjon av opioider og/eller benzodiazepiner ut over 24 timer, og insidensen øker til 80–100 prosent etter fem døgn med kontinuerlig infusjon (8). Abstinenssymptomer opptrer vanligvis innen 24–72 timer etter seponering av medikamentinfusjonen (4,8). Tilstanden gir ubehagelige symptomer fra flere organsystemer. De vanligste symptomene er nevrologiske symptomer, gastrointestinale symptomer og symptomer som skriver seg fra aktivering av det sympatiske nervesystemet (4). Diagnosen kan være vanskelig å stille siden symptomene kan sammenblandes med stress, smerte, tubeirritasjon eller delirium (9). På tross av at IA er en kjent problemstilling, er det i liten grad innarbeidet standardiserte overvåkings- og nedtrappingsplaner når det gjelder barn (1,10).
Forskning viser at bare 60 prosent av pediatriske pasienter er optimalt sedert (8,11). For å unngå abstinens ved nedtrapping, bør det benyttes et valid verktøy som tidlig kan avdekke symptomer på abstinens, slik at relevant behandling blir iverksatt (8). Sykepleiere som arbeider med barn trenger å kjenne til hvilke kartleggingsverktøy for iatrogen abstinens som er validert for denne pasientgruppen. Erfaringsmessig gir abstinenser et urolig barn, noe som kan være traumatisk for pårørende å oppleve. I tillegg kan det være utfordrende å være sykepleier hos et abstinent barn uten en nedtrappingsplan (12).
Et innledende litteratursøk avdekket at det finnes flere verktøy som kartlegger iatrogen abstinens (2). Verktøyene Withdrawal Assessment Tool-1 (WAT-1) (7) og Sophia Observation Withdrawal Symptoms Scale (SOS) (13) er validert for bruk på pediatriske pasienter og anbefalt av European Society of Paediatric and Neonatal Intensive Care (ESPNIC) (2). En skriftlig korrespondanse med de pediatriske intensivavdelingene i Norge i 2020, avdekket at WAT-1 blir benyttet ved Oslo universitetssykehus og St. Olavs hospital, og det ble informert om at flere barneavdelinger har tatt verktøyet i bruk.
Tidligere forskning har undersøkt symptomer og risikofaktorer ved IA (10), medikamenter som benyttes under nedtrapping av abstinens og bruk av avvenningsprotokoll (14), samt kartleggingsverktøy for IA og behandling av abstinenser hos den kritisk syke pediatriske pasienten (8). Konklusjonen i tidligere forskning er at kartleggingsverktøy for IA bør undersøkes for deres måleegenskaper. Dette kunnskapshullet vil vi dekke i vår systematiske oversikt ved å ta i bruk det metodiske rammeverket COnsensus-based Standards for the selection of health Measurement INstruments (COSMIN) for å kritisk vurdere måleegenskaper ved de ulike kartleggingsverktøyene (15).
Hensikten med denne systematiske oversikten er derfor 1) å identifisere hvilke kartleggingsverktøy som finnes for å identifisere iatrogen abstinens hos pediatriske pasienter, og 2) vurdere hvilke måleegenskaper disse kartleggingsverktøyene har. Vi vil undersøke om kartleggingsverktøyene er vurdert i forhold til måleegenskapene reliabilitet, validitet og responsivitet (15).
Metode
Studien er utført i henhold til PRISMA-S-sjekklisten for systematiske oversiktsartikler (16) og Muka og Glisics (17) 24 trinn for å planlegge, gjennomføre og publisere en systematisk oversikt. Vi har brukt COSMIN for å utføre kritisk vurdering av kartleggingsverktøyenes måleegenskaper, ekstrahere data og sammenstille data til en syntese (15). COSMIN er utarbeidet i en internasjonal konsensusprosess og gir spesifikke anbefalinger om terminologi, taksonomi og metodebruk i studier som skal vurdere måleegenskaper til kartleggingsverktøy.
Litteratursøk
Det ble i samråd med bibliotekar utført systematisk søk etter litteratur i databasene CINAHL (1981), Embase (1974–), MEDLINE (1946–), Epistemonikos (2012–), PubMed (1996–), SveMed+ (1977–) og Cochrane Library (1993–). Søkestrategien bestod av emneord og tekstord for kategoriene 1) pediatrisk pasient, 2) iatrogen abstinens og 3) kartleggingsverktøy. Vi brukte søkeordene pediatric, infant, child, newborn, iatrogenic, abstinence, withdrawal, opioid, opioids, benzodiazepine, assessment, score, method, tool, instrument og questionnaire. Søket ble gjennomført uten tidsbegrensing. Litteratursøk ble gjennomført i mars, mai og et siste suppleringssøk i oktober 2020. Vi kvalitetssikret søket med å screene referanselister til inkluderte studier og systematiske oversikter, og i tillegg søkte vi på verktøyenes navn. Inklusjons- og eksklusjonskriterier fremgår av tabell 1.
| Inklusjonskriterier | Eksklusjonskriterier | |
|---|---|---|
| Språk | Nordisk eller engelsk | Andre språk |
| Aldersgruppe | 0–18 år | > 18 år |
| Gjennomgått behandling | Sedasjon med benzodiazepiner og/eller opiater | |
| Kartleggingsverktøy | Skåringsverktøy for iatrogen abstinens | Skåringsverktøy for neonatalt abstinens syndrom (NAS), eller ingen skåring av abstinens |
| Artikkelformat | Tilgjengelig fulltekst | Ingen tilgang til fulltekst |
| Artikkeltype | Utviklingsstudier og valideringsstudier | Andre studier |
Utvelgelse
To personer (HH/KE) har uavhengig av hverandre screenet titler, sammendrag og fulltekst for inklusjon på bakgrunn av inklusjons- og eksklusjonskriterier (18). Ved uenighet ble en tredjepart involvert (MHR). Det ble utført pilottest på de første 50 studiene for å kvalitetssikre felles forståelse for kriteriene. Studier som beskriver kartleggingsverktøy og utvikling av kartleggingsverktøy for IA, og studier som evaluerer minst en måleegenskap innenfor kategoriene reliabilitet, validitet eller responsivitet, ble inkludert. Vi ekskluderte studier av barn født av mødre i Legemiddelassistert rehabilitering (LAR). Dette er en egen pasientgruppe som ofte utvikler neonatalt abstinenssyndrom (NAS), og som vurderes med egne spesialiserte kartleggingsverktøy.
COSMIN
COSMIN er valgt grunnet deres metodiske rammeverk for utarbeidelse av systematiske oversikter over måleegenskaper for kartleggingsverktøy, hovedsakelig Patient-Reported Outcome Measures (PROMs). PROMs er verktøy der pasienten selv vurderer og rapporterer sin egen status. Ettersom pediatriske pasienter i mindre grad kan vurdere og kommunisere sin egen situasjon, er verktøyene for å vurdere iatrogen abstinens hos denne pasientgruppen Clinician Reported Outcome Measurement (ClinROM). Dette er verktøy hvor pasientens helsepersonell vurderer og rapporterer barnets status. COSMIN-rammeverket er overførbart til ClinROM, men med noen tilpasninger (15).
Måleegenskaper
For å implementere nye kartleggingsverktøy på en arbeidsplass, er det viktig å forsikre seg om at verktøyene har gode måleegenskaper. Vi må vite at verktøyene måler det vi ønsker å finne ut, og om resultatene er gyldige og pålitelige (18). COSMIN deler måleegenskaper i tre hovedkategorier: reliabilitet, validitet og responsivitet. Reliabilitet handler om hvor stabile og konsise observasjonene er. Reliabilitet er et samlebegrep som favner intern konsistens, reliabilitet (test-retest, inter-rater og intra-rater reliabilitet) og målefeil. Validitet blir omtalt som gyldighet, og går ut på om kartleggingsverktøyets innhold reflekterer fenomenet som skal måles. Validitet består av innholdsvaliditet, begrepsvaliditet og kriterievaliditet. Innholdsvaliditet vurderes i forhold til begrepene relevans, fullstendighet og tydelighet. Relevans kan forklares ved at et kartleggingsverktøy for IA benyttes på pasienter man mistenker kan utvikle IA (18). Fullstendighet innebærer at verktøyet måler alt det er ment å måle, og kan vurderes ved at man ved pilottesting undersøker om relevante symptomer mangler, enten ved å spørre pasientene selv eller koble inn profesjonelle (18). Tydelighet innebærer at det er en tydelig instruks og forståelige formuleringer og spørsmål i kartleggingsverktøyet (15). Begrepsvaliditet består av strukturell validitet, hypotesetesting og tverrkulturell validitet. Strukturell validitet beskriver om kartleggingsverktøyet reflekterer fenomenets dimensjoner, og faktoranalyse benyttes for å undersøke om kartleggingsverktøyet består av en eller flere dimensjoner. Ved utviklingsstudier benyttes utforskende faktoranalyse, mens ved senere anledninger benyttes bekreftende faktoranalyse (18). Hypotesetesting undersøker om retning og størrelse på en samvariasjon eller forskjell er som forventet ut fra fenomenet som måles. Tverrkulturell validitet undersøker om en oversatt versjon av kartleggingsverktøyet fungerer på samme måte som den originale versjonen. Oversettelsesprosessen er del av den tverrkulturelle validiteten og bør følge internasjonale retningslinjer for frem- og tilbakeoversettelse (19). Responsivitet er evnen kartleggingsverktøyet har til å oppdage endringer over tid (15,18), som symptomer på abstinens i vårt tilfelle.
Sjekkliste for å vurdere metodisk kvalitet
For å vurdere metodisk kvalitet og risiko for feilmålinger har vi benyttet sjekklisten fra COSMIN, Risk of Bias Checklist (15). Sjekklisten består av ti bokser, der hver boks gir en kvalitetsvurdering av en måleegenskap. Boks 1 tar for seg verktøyutvikling, boks 2 ser på innholdsvaliditet og boks 3–10 vurderer de ulike måleegenskapene. Metodisk kvalitet vurderes til inadekvat, tvilsom, adekvat eller svært god, eventuelt ikke aktuell. En samlet skår for hver boks fastsettes etter prinsippet om at dårligste skår teller. Alle kvalitetsvurderinger er gjennomført av to personer (HH/KE) uavhengig av hverandre. Uenighet er løst ved diskusjon eller ved involvering av en tredje person (MHR).
Dataekstraksjon og kategorisering av måleegenskaper
Registrering av karakteristika ved hver studie er foretatt av to personer uavhengig av hverandre på bakgrunn av et forhåndsdefinert dataekstraksjonsskjema (15). Måleegenskapene til det aktuelle kartleggingsverktøyet ble vurdert som tilstrekkelig (+), utilstrekkelig (–) eller ubestemmelig (?) opp mot forhåndsdefinerte kriterier. Vi sammenstilte funnene og vurderingene av måleegenskapene til kartleggingsverktøyene i en syntese som tar hensyn til metodisk kvalitet, måleegenskaper og grad av konsistens. Hver vurdering blir etterfulgt av en vurdering av evidenskvalitet, som forteller hvor stor tillit man kan ha til vurderingen. Evidenskvalitet blir vurdert til høy, moderat, lav eller svært lav.
Resultater
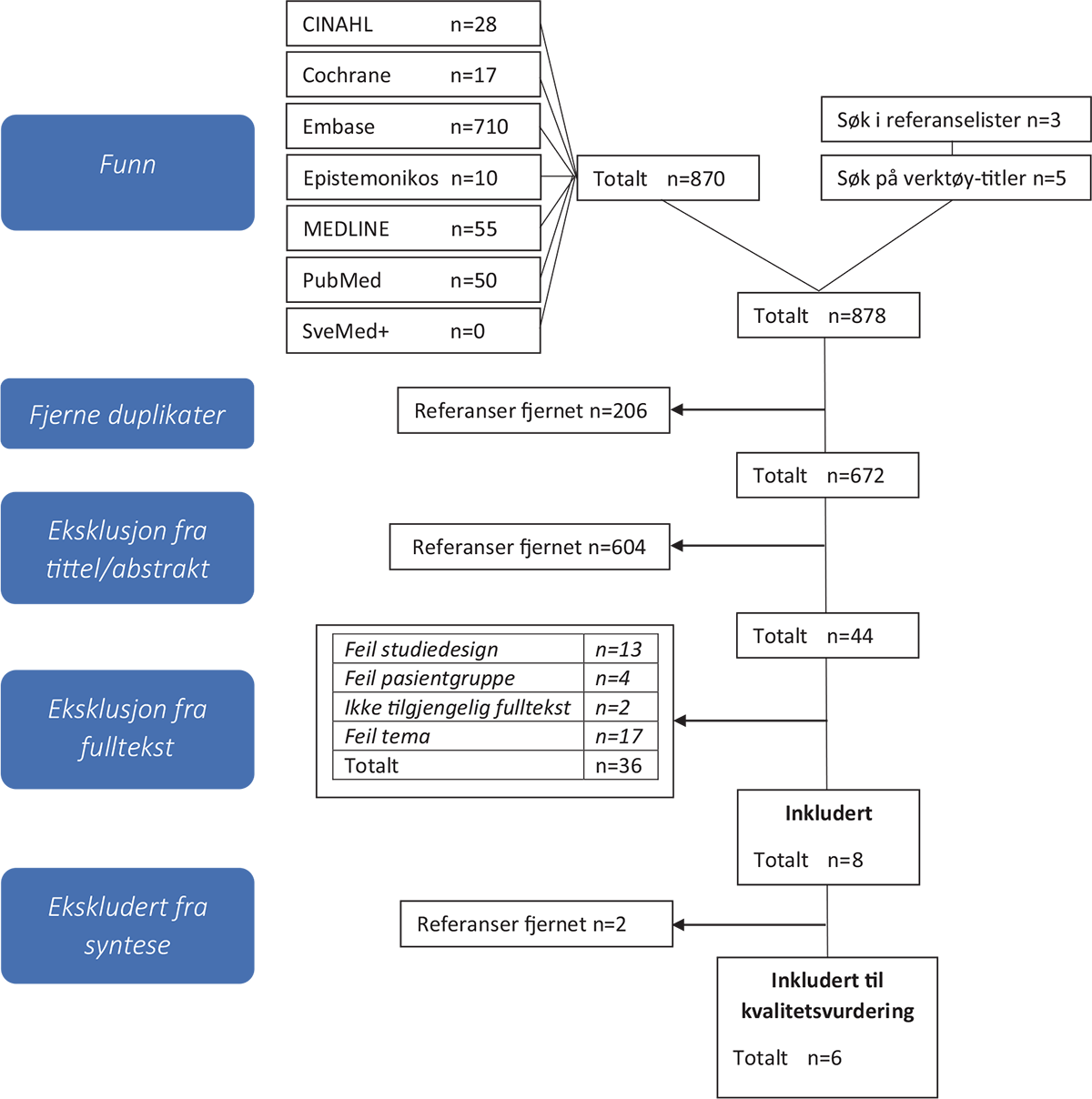
Det strukturerte litteratursøket (figur 1) gav oss 878 referanser, og vi inkluderte åtte studier (5,7,13,20–24). Vi identifiserte seks kartleggingsverktøy for IA for barn opp til 18 år: Sedation Withdrawal Score (SWS), Sophia Observation withdrawal Symptoms- Pediatric Delirium scale (SOS-PD), Opiate and Benzodiazepine Withdrawal Score (OBWS), Withdrawal Assessment Tool-1 (WAT-1), Sophia Observation withdrawal Symptoms-scale (SOS), og Adjusted Finnegan (tabell 2).
Karakteristika ved hvert kartleggingsverktøy
Av de seks identifiserte kartleggingsverktøyene for iatrogen abstinens hos barn, er det to verktøy som ikke inngår i syntesen for måleegenskaper, dette gjelder SWS og SOS-PD. Studien som beskriver utviklingen av SWS (20) er en casestudie av bare én pasient, og SOS-PD (21) er en nyere utgave av SOS, men hvor det legges til kartlegging med tanke på delirium. Ettersom vi ikke har fokusert på delirium, har vi ikke vurdert SOS-PD gjennom COSMIN.
Tabell 3 viser hvilke symptomer som kartlegges i de ulike verktøyene. Symptomene er oversatt fra engelsk, og noen av symptomene går noe over i hverandre. I originalversjonene følger tekst som beskriver mer utdypende hva hvert enkelt symptom innebærer.
| Verktøy | Poeng | Tidsbruk | Dimensjoner |
|---|---|---|---|
| SWS | 0–24 poeng | Ikke angitt | 3 dimensjoner
– CNS irritabilitet – Gastrointestinale symptomer – Autonom dysfunksjon |
| OBWS | 0–16 poeng | Ikke angitt | Ikke angitt |
| WAT-1 | 0–12 poeng | Ca. 7 min | 4 dimensjoner
– Motoriske symptomer – Atferdstilstand før stimulering – Autonom dysfunksjon – Gastrointestinale symptomer |
| SOS | 0–15 poeng | Ca. 2 min | 3 dimensjoner
– Gastrointestinale symptomer – CNS irritabilitet – Autonom dysfunksjon |
| SOS-PD | 0–17 poeng | Ikke angitt | Ikke angitt |
| Adjusted Finnegan | 0–31 poeng | Ikke angitt | Ikke angitt |
| Symptomer på abstinens | SWS | OBWS | WAT-1 | SOS | SOS-PD | A.F. | |
|---|---|---|---|---|---|---|---|
| Sympatisk aktivering | Svetting | x | x | x | x | x | x |
| Gjesping/nysing | x | x/x | x | x/x | |||
| Takykardi | x | ||||||
| Takypné/respirasjonsproblem | x | x | x | ||||
| Dilaterte pupiller | x | ||||||
| Nevrologiske symptomer | Hallusinasjoner | x | x | x | |||
| Våkenhetsgrad | x | ||||||
| Skjelvinger/rykninger | x | x | x | x | x | x | |
| Motorisk uro / kramper | x/x | x | x | x | |||
| Agitasjon/irritasjon | x | x | x | x | |||
| Feber | x | x | x | x | |||
| Angstpreget uttrykk | x | x | |||||
| Grimasering | x | x | |||||
| Gråt, utrøstelig/høytonet | x | x/x | x | x | x | ||
| Anspent / økt muskeltonus | x | x | x | x | x | ||
| Ukoordinerte/gjentagende bevegelser | x | ||||||
| Avbrutt søvnmønster | x | x | x | ||||
| Mororefleks | x | ||||||
| Gastro | Kvalme/oppkast/gulp | x | x | x | x | x | |
| Diaré/løs/vandig avføring | x | x | x | x | x | ||
| Annet | Tett nese | x | |||||
| Hyppig sug | x | ||||||
| Reaksjon på berøring | x | ||||||
| Tid til ro etter berøring | x | ||||||
| Marmorering | x | ||||||
| Delirspesifikke | Fokus/apati | x | |||||
| Bevisst handling | x | ||||||
| Manglende øyekontakt | x | ||||||
| Forvirring | x | ||||||
| Usammenhengende tale | x | ||||||
| Akutt endrede symptomer | x | ||||||
| Svingninger i symptomer | x |
OBWS
Verktøyet beskrives som en videreutvikling av Opioid Withdrawal Flowsheet fra 1995, utviklet for å vurdere abstinens hos barn (22). Studien er en prospektiv repeterende studie som ble gjennomført over en 11 måneders periode på pasienter i alderen fra 6 uker opp til 28 måneder. På bakgrunn av valideringsstudien alene kan ikke verktøyutviklingen vurderes. Når det gjelder validitet, er det målt sensitivitet på 50 prosent og spesifisitet på 87 prosent, og det angis en inter-rater-reliabilitet på 80 prosent. Verktøyet beskrives som å «inneholde mange elementer», og 17 symptomer er presentert i artikkelen. Utviklerne påpekte at verktøyet ikke var pålitelig nok (22). Studien er vurdert gjennom COSMINs sjekkliste for relevans og fullstendighet. Begge ble vurdert som tvilsom, hovedsakelig fordi det ikke var mulig å vurdere utviklingen av OBWS basert på informasjonen i denne studien. Total relevans og total fullstendighet endte som ubestemmelig med svært lav evidens, noe som medfører ubestemmelig innholdsvaliditet med svært lav evidens (tabell 4).
WAT-1
Verktøyet ble utarbeidet med bakgrunn i at forgjengeren, OBWS, manglet spesifisitet, sensitivitet og brukervennlighet for bruk på pediatriske pasienter med IA (7). Basert på OBWS, litteratursøk og eksperterters mening ble det plukket ut 19 symptomer som skulle avdekke symptomene på abstinens. Symptomene ble utprøvd og vurdert og satt sammen til et sluttresultat på en 11-punkts skala. Korrelasjonen mellom de 19 opprinnelige symptomene og verktøyet WAT-1 var 0,947. Dersom en pasient skåres til tre poeng eller mer, regnes dette som abstinens. Det foreligger to multisenterstudier, hvorav en er en utviklingsstudie og en er en valideringsstudie (7,23). Utviklingsstudien ble testet ut på to pediatriske intensivavdelinger og valideringsstudien på 22 pediatriske intensivavdelinger. Pasientgruppene var pediatriske pasienter som var eksponert for benzodiazepiner og opioider i fem eller flere dager. Basert på de nevnte studiene vurderes innholdsvaliditeten til WAT-1 som svært god, og ved bruk av COSMINs sjekklister vurderes verktøyutviklingen som svært god. Inter-rater-reliabilitet målt ved Cohens kappa viste 0,8. Det ble utført utforskende faktoranalyse i utviklingsstudien og bekreftende faktoranalyse i valideringsstudien, noe som gjennom COSMIN gir høy strukturell validitet. Kartleggingsverktøyet består av fire dimensjoner (tabell 2). Samlet sett vurderes reliabilitet og begrepsvaliditet som adekvat for begge studiene. Total reliabilitet og total begrepsvaliditet er vurdert til adekvat med høy evidenskvalitet (tabell 4). Pasientgruppen med skåringer over tre ble sammenlignet med gruppen som hadde skår under tre. Det ble også sammenlignet forekomst av symptomer i de ulike aldersgruppene. Studiene fant at pasienter med abstinens hadde lengre liggetid, lengre opioideksponering og lengre avvenningstid (7,23). Utviklingsstudien har i tillegg testet responsivitet ved Area Under the Receiver Operating Characteristic (AUROC) og Numerical Rating Scale (NRS). Ved NRS skåret helsepersonell abstinens basert på subjektive vurderinger på en skala fra 0–10. Sammenligning mellom AUROC og NRS fant en svært høy spesifisitet (0,88) og sensitivitet (0,87), men det påpekes at verktøyet i høyere grad fanger opp abstinenssymptomer for opioider enn for benzodiazepiner (7). WAT-1 er oversatt til mange språk, deriblant norsk (6,25). Oversettelsesprosessen inngår som en del av den tverrkulturelle validiteten. Vi har imidlertid ikke lykkes med å finne publiserte norske studier som beskriver selve oversettelsesprosessen for WAT-1, men en studie av Dokken (6) rapporterer at oversettelsesprosessen fulgte protokoll for frem-og-tilbake-oversettelse.
SOS
SOS ble utformet av kliniske eksperter i Nederland i 2009 (13). Verktøyet ble utviklet basert på begrensninger i daværende kartleggingsverktøy som ble vurdert til å ha moderat validitet. På bakgrunn av litteratursøk ble symptomer satt sammen til et midlertidig verktøy som ble prøvd ut på pasientene. Et ekspertpanel bestående av intensivleger og intensivsykepleiere vurderte klinisk relevans for hvert av symptomene. Alle symptomer med skår under 0,65 på Cohens kappa ble fjernet fra listen. Sluttresultatet ble et kartleggingsverktøy bestående av 15 symptomer (13). Inter-rater-reliabilitet for de gjenværende symptomene ble målt til mellom 0,73 og 1,0. Verktøyutviklingen vurderes til svært god på bakgrunn av utviklingsstudien (tabell 4). Intraklassekorrelasjon (ICC) mellom vakthavende sykepleier og forsker ble målt til 0,97 og reliabiliteten ble av utviklerne selv vurdert som god. Ved hjelp av COSMIN vurderes reliabiliteten som tilstrekkelig, med moderat evidens. Av de to SOS-studiene (5,13) er det ingen som har testet tydelighet, men relevans er vurdert til adekvat. Total innholdsvaliditet vurderes til adekvat med høy evidenskvalitet (tabell 4). Det fremkom tre dimensjoner ved utforskende faktoranalyse (13). Hypotesetesting ble utført ved å sammenligne grupper, hvor en gruppe bestod av pasienter med få symptomer på IA, og den andre gruppen av pasienter med høyere grad av abstinens. SOS ble korrelert mot NRS, som resulterte i en korrelasjonskoeffisient på 0,78. Det ble utført analyser for å vurdere hvor sensitivt verktøyet var til å fange opp endringer i symptomer og effekt av behandling. Resultatet var et fall i 1,5 poeng etter iverksetting av behandlingstiltak, og studien angir en sensitivitet på 0,83 og en spesifisitet på 0,93 (5). Verktøyet kan benyttes etter eksponering for både opioider og benzodiazepiner (4), men utviklerne av SOS påpeker at deres verktøy er mer sensitivt for benzodiazepiner enn WAT-1 (5). SOS beskrives som fremragende når det gjelder å forutse hvilke pasientgrupper som ikke vil utvikle IA. Negativ prediktiv verdi angis til 0,98, mens positiv prediktiv verdi viste seg å være lav, noe som kan komme av at symptomer på abstinens kan forveksles med smerte, stress og delirium (1,5).
Adjusted Finnegan
Adjusted Finnegan (24) er en videreutvikling av Modified Finnegan, som er et kartleggingsverktøy for neonatalt abstinenssyndrom. For å gjøre verktøyet relevant for eldre barn ble verktøyet justert ved å fjerne typiske nyfødt-symptomer, som eksempelvis mororefleks, og verktøyet fikk navnet Adjusted Finnegan (24). Verktøyutvikling blir vurdert til tvilsom ettersom det ikke er beskrevet noen form for strategi for hvilke symptomer som skal inkluderes. Total relevans og total tydelighet blir vurdert til adekvat til tross for at fullstendighet blir vurdert til ubestemmelig. Evidenskvaliteten ble vurdert til svært lav (tabell 4).
| OBWS | WAT-1 | SOS | Adjusted Finnegan | |||||
|---|---|---|---|---|---|---|---|---|
| Oppsummert Vurdering | Evidenskvalitet | Oppsummert Vurdering | Evidenskvalitet | Oppsummert Vurdering | Evidenskvalitet | Oppsummert Vurdering | Evidenskvalitet | |
| + / – / ? | Høy, moderat, lav, svært lav | + / – / ? | Høy, moderat, lav, svært lav | + / – / ? | Høy, moderat, lav, svært lav | + / – / ? | Høy, moderat, lav, svært lav | |
| Innholdsvaliditet | ? | Svært lav | + | Høy | + | Høy | + | Svært lav |
| Relevans | ? | Svært lav | + | Høy | + | Moderat | + | Svært lav |
| Fullstendighet | + | Moderat | + | Høy | ? | Svært lav | ||
| Tydelighet | ? | Svært lav | + | Moderat | + | Moderat | + | Svært lav |
| Strukturell validitet | + | Høy | + | Moderat | ||||
| Intern konsistens | ||||||||
| Tverrkulturell validitet | ||||||||
| Reliabilitet | + | Svært lav | + | Høy | + | Moderat | ||
| Målefeil | + | Svært lav | ||||||
| Kriterievaliditet | ||||||||
| Begrepsvaliditet | + | Svært lav | + | Høy | + | Høy | + | Svært lav |
| Responsivitet | + | Moderat | + | Moderat | ||||
+ Tilstrekkelig – Utilstrekkelig ? Ubestemmelig
Diskusjon
Hensikten med denne systematiske oversikten var å identifisere hvilke kartleggingsverktøy som finnes for IA hos pediatriske pasienter, og å vurdere verktøyenes måleegenskaper. Vi fant åtte studier som beskriver seks kartleggingsverktøy for iatrogen abstinens hos pediatriske pasienter. I henhold til inkluderingskriteriene er fire kartleggingsverktøy vurdert ved bruk av COSMIN og sammenstilt i en syntese. Tre av studiene evaluerer både kartleggingsverktøyets utvikling og validering. Oppsummert vurderer alle studiene begrepsvaliditet, fire studier vurderer innholdsvaliditet og to studier vurderer responsivitet. Ingen studier vurderer tverrkulturell validitet eller intern konsistens med måling av Cronbachs alfa. WAT-1 er oversatt til norsk (25) og benyttes i pediatriske intensivavdelinger og barneavdelinger. Imidlertid har vi ikke lykkes å finne studier som beskriver selve oversettelsesprosessen og valideringen av verktøyet til en norsk kontekst. OBWS og Adjusted Finnegan blir vurdert til å ha svært lav evidenskvalitet, som betyr at en kan ha mindre tillit til resultatene. De svake resultatene kommer fra metodene brukt for å vurdere måleegenskapene, i tillegg til studier med få deltakere. Multisenterstudier bidrar til at det totale utvalget blir større, slik at mer robuste analysemetoder kan utføres, noe som er ivaretatt ved utvikling av WAT-1. WAT-1 og SOS har høy eller moderat evidenskvalitet for alle sine måleegenskaper, noe som betyr at man kan tillegge resultatene tillit. Dette er i samsvar med funnene i studien til Harris et al. (2), der disse to verktøyene er anbefalt av ESPNIC som kartleggingsverktøy for IA.
En litteraturstudie fra 2020 konkluderte med at det var tre validerte verktøy for å kartlegge IA: OBWS, WAT-1 og SOS (8). Ved hjelp av COSMIN finner vi at OBWS sin innholdsvaliditet vurderes til ubestemmelig. OBWS er det eneste verktøyet som har med «mororefleks» som symptom, hvilket er en refleks som kun er aktuell for spedbarn under tre måneder (8). Dette er det imidlertid tatt høyde for i WAT-1, som har bygget videre på OBWS, ved at det her ikke er aldersspesifikke symptomer eller reflekser. Imidlertid stiller Ávila-Alzate et al. (8) spørsmål ved om kartleggingsverktøy for iatrogen abstinens hos pediatriske pasienter kan favne hele aldersspennet fra 0–18 år, og foreslår at det må utvikles verktøy for IA som tilpasses de ulike alderskategoriene for barn.
I vår syntese har den metodiske kvaliteten til enkeltstudiene og måleegenskapene til kartleggingsverktøyene blitt satt sammen for å vurdere evidenskvalitet. COSMIN (15) vektlegger relevans, fullstendighet og tydelighet for å vurdere innholdsvaliditet. WAT-1 (7) og SOS (13) blir vurdert til å ha god innholdsvaliditet ettersom symptomenes relevans er vurdert av leger og sykepleiere som er eksperter på området. Adjusted Finnegan (24) har tatt utgangspunkt i målinger for nyfødte, og valgt å fjerne symptomer for nyfødtes mororeflekser. For OBWS (22) er det uavklart hvordan de har kommet frem til kartleggingsverktøyets innhold. Det er derfor ikke mulig å vurdere fullstendighet, men på bakgrunn av relevans og tydelighet har det vært mulig å gi en vurdering av innholdsvaliditet, men evidenskvaliteten vurderes til meget lav.
Begrepsvaliditet hos hvert enkelt kartleggingsverktøy er avhengig av strukturell validitet, tverrkulturell validitet og hypotesetesting. Adjusted Finnegan (24) er utviklet ved en enkel justering av verktøyet Modified Finnegan. COSMIN-metoden krever imidlertid at videreutviklede verktøy blir behandlet som nye verktøy (15). Ettersom vi baserer måleegenskapene til Adjusted Finnegan og OBWS på en studie hver, er datagrunnlaget mangelfullt for flere av måleegenskapene i COSMIN, noe som medfører begrenset tillit til verktøyenes strukturelle validitet. WAT-1 og SOS vurderes begge med utforskende faktoranalyse i sine utviklingsstudier. I valideringsstudiene benytter WAT-1 bekreftende faktoranalyse og SOS multidimensjonal skalering. Dette, sammen med kravet om minst 100 deltagere når en skal vurdere strukturell validitet, gir god tillit til at disse to verktøyenes strukturelle validitet er tilstrekkelig. Hypotesetesting ble utført for WAT-1 og SOS, både mellom pasientgrupper og ved sammenligning med andre verktøy. Det er en styrke at det fremsettes hypoteser for å redusere risikoen for systematiske skjevheter (18).
Reliabiliteten til både WAT-1 og SOS er god. Inter-rater-reliabilitet er testet før og underveis i studiene. Det fremkommer i studiene at både WAT-1 og SOS har tilfredsstillende resultat for sensitivitet og spesifisitet, noe som er viktig for at verktøyet kan diskriminere mellom syke og friske, eller mellom de som har tilstanden og de som ikke har tilstanden (18). Imidlertid påpekes det at WAT-1 er mindre sensitiv for å fange opp symptomer etter behandling med benzodiazepiner enn etter behandling med opioider, sammenlignet med SOS (7). Dette kan skyldes at WAT-1, i motsetning til SOS og OBWS, ikke vurderer symptomer som hallusinasjoner, grimaser og betydelige uorganiserte bevegelser som disse legemidlene kan gi (8). Tilsvarende påstår utviklerne av SOS at deres kartleggingsverktøy i større grad fanger opp symptomer etter behandling med benzodiazepiner enn WAT-1 gjør (5).
Våre resultater viser at både WAT-1 og SOS har flere gode måleegenskaper. Begge verktøyene har god evidenskvalitet og er begge egnede verktøy å bruke til å identifisere IA hos pediatriske pasienter. WAT-1 angir å fange opp symptomer på IA uavhengig av alder (7). Imidlertid vil studier som vurderer flere måleegenskaper ved WAT-1 og SOS være ønskelig i fremtidig forskning for å kunne bidra med utvidet kunnskap om verktøyenes egnethet. At enkelte måleegenskaper ikke blir vurdert betyr ikke at måleegenskapene er dårlige, men at de er uavklarte og at det er behov for ytterligere utprøving. Selv om vi finner at flere av verktøyene er oversatt til ulike språk, beskriver ikke studiene selve oversettelsesprosessen. Dette er noe som slår negativt ut i COSMIN ved at det påvirker vurdering av tverrkulturell validitet. Det anbefales at forskningsstudier synliggjør hvordan de har oversatt og krysskulturelt tilpasset nye spørreskjemaer til konteksten instrumentet skal benyttes i og at tidsskrifter tillater at dette blir publisert for å styrke tverrkulturell validitet (26).
Styrker og svakheter ved studien
I samråd med bibliotekar brukte vi en bred søkestrategi for å fange opp studier som beskrev kartleggingsverktøy for IA og deres måleegenskaper. Vi brukte ingen begrensende søkeord i forhold til måleegenskaper. Det ble gjennomført suppleringssøk før ferdigstillelse av oversikten, noe som er anbefalt (27). Vi har derimot ekskludert alle språk utenom nordisk og engelsk, og vi har ikke søkt i grå litteratur, noe som kunne ha identifisert ytterligere relevante studier (27). Under utarbeidelsen av denne artikkelen ble det publisert en systematisk oversikt som har sett på behandling av IA (8). Vi sammenlignet vår studie med denne og fant ingen relevante referanser i deres referanseliste som vi ikke allerede hadde funnet. Imidlertid fant vi to artikler som var publisert i etterkant av deres litteratursøk, og disse artiklene representerer verktøyene SOS-PD (21) og Adjusted Finnegan (24).
I en systematisk oversikt anbefales det at alle steg i utvelgelsesprosessen av studier blir screenet av minst to personer uavhengig av hverandre. I tillegg til dette har vi søkt hjelp hos en tredjepart ved usikkerhet, i tråd med anbefalinger (17). Dette har redusert risikoen for at relevante studier er ekskludert fra den systematiske oversikten. Utvelgelsen og kvalitetsvurderingen er pilottestet, noe som anbefales for å styrker studiens kvalitet (18).
Dataekstraksjon, kvalitetsvurdering av studier og vurdering av måleegenskaper ble gjort med bruk av det kvalitetssikrede rammeverket COSMIN, som gir et standardisert vurderingsgrunnlag ved utarbeidelse av systematiske oversikter over måleegenskaper (15). Selv om COSMIN kan anvendes på ClinROM, møtte vi på noen utfordringer ettersom brukermanualen og spørsmålene er tilpasset PROMs. Vi erfarte at det var behov for en god forståelse av både PROMs og ClinROM for å kunne vurdere hvilke tilpasninger som måtte gjøres. COSMIN holder på å utvikle egne verktøy for ClinROM, men dette verktøyet var ikke publisert under vår utarbeidelse av denne systematiske oversikten. COSMIN kan med fordel anbefales som veileder for nye valideringsstudier, og det vil være av interesse å gjøre en ny vurdering av kartleggingsverktøyenes måleegenskaper når COSMIN publiserer sin ClinROM-sjekkliste.
Implikasjoner for praksis og videre forskning
Håndtering av IA-abstinens kan ikke finne sted med mindre abstinens først oppdages, noe et validert og pålitelig kartleggingsverktøy kan bidra til. En prospektiv observasjonsstudie som benyttet SOS fant at eksponering for opioider og benzodiazepiner i mer enn tre dager kunne gi symptomer på IA. Studien fant også at barn med IA hadde behov for lengre tid på mekanisk ventilasjon, krevde en lengre periode med avvenning av medikamenter og hadde generelt lengre sykehusopphold (28). En implementeringsstudie av WAT-1 fant at den tverrfaglige kommunikasjonen mellom sykepleiere og leger ble mer presis, og at sykepleierne opplevde større tilfredshet med kvaliteten på pleie og behandling (12). Dette viser hvor viktig det er å benytte et validert verktøy for tidlig å fange opp IA og kunne iverksette tiltak.
Implementeringsforskning har vist at vellykket implementering av kartleggingsverktøy er mulig (12). Forskningen understreker viktigheten av et utdanningsprogram der det gis opplæring i hvordan kartleggingsverktøyet skal brukes, supplert med individuell oppfølging og tilbakemelding til helsepersonell ved bruk av verktøyet på pasienter (29). Tilsvarende forskning på implementering av kartleggingsverktøy for delir har vist at det også er viktig å diskutere resultatet fra kartleggingen på legevisitter og å dokumentere resultat av kartleggingen i elektroniske dokumentasjonssystemer (30). For vellykket implementering av kartleggingsverktøy i en arbeidshverdag er det også viktig at verktøyene er brukervennlige (12). Dette innebærer blant annet å ha korte og konsise spørsmål som besvares uten rom for feiltolkning, og at kartleggingen er rask å utføre (31). I så måte skiller SOS seg best ut med en angitt utfyllingstid på to minutter sammenlignet med WAT-1, som oppgir en utfyllingstid på syv minutter. WAT-1 er allerede oversatt til norsk, men vi har ikke lykkes å finne studier som har oversatt SOS til norsk.
Konklusjon
Vi identifiserte seks kartleggingsverktøy for iatrogen abstinens for barn opp til 18 år: SWS (Sedation Withdrawal Score), SOS-PD (Sophia Observation withdrawal Symptoms- Pediatric Delirium scale), OBWS (Opiate and Benzodiazepine Withdrawal Score), WAT-1 (Withdrawal Assessment Tool-1), SOS (Sophia Observation withdrawal Symptoms-scale), og Adjusted Finnegan. Fire av verktøyene er vurdert for måleegenskaper ved bruk av det metodiske rammeverket COSMIN. Av disse vurderes WAT-1 og SOS til å ha gode måleegenskaper og god evidenskvalitet. Fremtidige studier kan imidlertid vurdere flere måleegenskaper ved kartleggingsverktøyene for å få et sterkere evidensgrunnlag. Det er ønskelig at fremtidig forskning dokumenterer oversettelsesprosedyre og validering av verktøyene WAT-1 og SOS til en norsk kontekst.
Referanser
- 1. Neunhoeffer F, Kumpf M, Renk H, Hanelt M, Berneck N, Bosk A, et al. Nurse-driven pediatric analgesia and sedation protocol reduces withdrawal symptoms in critically ill medical pediatric patients. Pediatr Anesth. 2015;25(8):786–94. https://doi.org/10.1111/pan.12649
- 2. Harris J, Ramelet A-S, van Dijk M, Pokorna P, Wielenga J, Tume L, et al. Clinical recommendations for pain, sedation, withdrawal and delirium assessment in critically ill infants and children: an ESPNIC position statement for healthcare professionals. Intensive Care Med. 2016;42(6):972–86. https://doi.org/10.1007/s00134-016-4344-1
- 3. Weis JK, Riiser CW. Klinisk retningslinje for vurdering af iatrogene abstinenser hos børn fra 28 uge til 3 år indlagt til intensiv terapi [Internett]. Aalborg Universitet: Institut for Medicin og Sundhedsteknologi; 2018. Tilgjengelig fra: https://cfkr.dk/retningslinjer/godkendte-retningslinjer/klinisk-retningslinje-for-vurdering-af-iatrogene-abstinenser-hos-boern-fra-28-dage-3-aar-indlagt-til-intensiv-terapi/
- 4. Duceppe MA, Perreault MM, Frenette AJ, Burry LD, Rico P, Lavoie A, et al. Frequency, risk factors and symptomatology of iatrogenic withdrawal from opioids and benzodiazepines in critically ill neonates, children and adults: a systematic review of clinical studies. J Clin Pharm Ther. 2019;44(2):148–56. https://doi.org/10.1111/jcpt.12787
- 5. Ista E, de Hoog M, Tibboel D, Duivenvoorden HJ, van Dijk M. Psychometric evaluation of the Sophia Observation withdrawal symptoms scale in critically ill children. Pediatr Crit Care Med. 2013;14(8):761–9. https://doi.org/10.1097/PCC.0b013e31829f5be1
- 6. Dokken M, Rustøen T, Diep LM, Fagermoen FE, Huse RI, A. Rosland G, et al. Iatrogenic withdrawal syndrome frequently occurs in paediatric intensive care without algorithm for tapering of analgosedation. Acta Anaesthesiol Scand. 2021. https://doi.org/10.1111/aas.13818
- 7. Franck LS, Harris SK, Soetenga DJ, Amling JK, Curley MA. The Withdrawal Assessment Tool-Version 1 (WAT-1): an assessment instrument for monitoring opioid and benzodiazepine withdrawal symptoms in pediatric patients. Pediatr Crit Care Med. 2008;9(6):573. https://doi.org/10.1097/PCC.0b013e31818c8328
- 8. Ávila-Alzate JA, Gómez-Salgado J, Romero-Martín M, Martínez-Isasi S, Navarro-Abal Y, Fernández-García D. Assessment and treatment of the withdrawal syndrome in paediatric intensive care units: systematic review. Medicine. 2020;99(5). https://doi.org/10.1097/MD.0000000000018502
- 9. Polaner DM. Sedation-analgesia in the pediatric intensive care unit. Pediatr Clin North Am. 2001;48(3):695– 714. https://doi.org/10.1016/S0031-3955(05)70335-7
- 10. Birchley G. Opioid and benzodiazepine withdrawal syndromes in the paediatric intensive care unit: a review of recent literature. Nurs Crit Care. 2009;14(1):26–37. https://doi.org/10.1111/j.1478-5153.2008.00311.x
- 11. Vet NJ, Ista E, de Wildt SN, van Dijk M, Tibboel D, de Hoog M. Optimal sedation in pediatric intensive care patients: a systematic review. Intensive Care Med. 2013;39(9):1524–34. https://doi.org/10.1007/s00134-013-2971-3
- 12. Suddaby EC, Josephson K. Satisfaction of nurses with the Withdrawal Assessment Tool-1 (WAT-1). Pediatr Nurs. 2013;39(5):238.
- 13. Ista E, van Dijk M, de Hoog M, Tibboel D, Duivenvoorden HJ. Construction of the Sophia Observation withdrawal Symptoms-scale (SOS) for critically ill children. Intensive Care Med. 2009;35(6):1075–81. https://doi.org/10.1007/s00134-009-1487-3
- 14. Chiu AW, Contreras S, Mehta S, Korman J, Perreault MM, Williamson DR, et al. Iatrogenic opioid withdrawal in critically ill patients: a review of assessment tools and management. Ann Pharmacother. 2017;51(12):1099–111. https://doi.org/10.1177/1060028017724538
- 15. Mokkink LB, De Vet HC, Prinsen CA, Patrick DL, Alonso J, Bouter LM, et al. COSMIN risk of bias checklist for systematic reviews of patient-reported outcome measures. Qual Life Res. 2018;27(5):1171–9. https://doi.org/10.1007/s11136-017-1765-4
- 16. Moher D, Liberati A, Tetzlaff J, Altman DG. Preferred reporting items for systematic reviews and meta-analyses: the PRISMA statement. Int J Surg. 2010;8(5):336–41. https://doi.org/10.1016/j.ijsu.2010.02.007
- 17. Muka T, Glisic M, Milic J, Verhoog S, Bohlius J, Bramer W, et al. A 24-step guide on how to design, conduct, and successfully publish a systematic review and meta-analysis in medical research. Eur J Epidemiol. 2020;35(1):49–60. https://doi.org/10.1007/s10654-019-00576-5
- 18. De Vet HC, Terwee CB, Mokkink LB, Knol DL. Measurement in medicine: a practical guide. Cambridge: Cambridge University Press; 2017.
- 19. Polit DF, Beck CT. Nursing research: generating and assessing evidence for nursing practice. Philadelphia: Wolters Kluwer; 2017.
- 20. Cunliffe M, McArthur L, Dooley F. Managing sedation withdrawal in children who undergo prolonged PICU admission after discharge to the ward. Pediatr Anesth. 2004;14(4):293–8. https://doi.org/10.1046/j.1460-9592.2003.01219.x
- 21. Ista E, Te Beest H, van Rosmalen J, de Hoog M, Tibboel D, van Beusekom B, et al. Sophia Observation withdrawal Symptoms-Paediatric Delirium scale: a tool for early screening of delirium in the PICU. Aust Crit Care. 2018;31(5):266–73. https://doi.org/10.1016/j.aucc.2017.07.006
- 22. Franck LS, Naughton I, Winter I. Opioid and benzodiazepine withdrawal symptoms in paediatric intensive care patients. Intensive Crit Care Nurs. 2004;20(6):344–51. https://doi.org/10.1016/j.iccn.2004.07.008
- 23. Franck LS, Scoppettuolo LA, Wypij D, Curley MA. Validity and generalizability of the Withdrawal Assessment Tool-1 (WAT-1) for monitoring iatrogenic withdrawal syndrome in pediatric patients. Pain. 2012;153(1):142–8. https://doi.org/10.1016/j.pain.2011.10.003
- 24. Capino AC, Johnson PN, Williams PK, Anderson MP, Bedwell S, Miller JL. Pilot study comparing modified Finnegan Scoring versus adjusted scoring system for infants with iatrogenic opioid abstinence syndrome after cardiothoracic surgery. J Pediatr Pharmacol Ther. 2019;24(2):148–55. https://doi.org/10.5863/1551-6776-24.2.148
- 25. Scheen SIF LA. Withdrawal assessment tool version 1 (WAT-1) [Internett]. Oslo: Oslo universitetssykehus Rikshospitalet; 2011. Tilgjengelig fra: http://www.norskbarnesmerteforening.no/sites/norskbarnesmerteforening.no/files/attachments/articles/WAT-1%20norsk%20versjon-2%20Sheet1.pdf
- 26. Sousa VD, Rojjanasrirat W. Translation, adaptation and validation of instruments or scales for use in cross-cultural health care research: a clear and user-friendly guideline. J Eval Clin Pract. 2011;17(2):268–74. https://doi.org/10.1111/j.1365-2753.2010.01434.x
- 27. Nylenna M. Slik oppsummerer vi forskning [Internett]. Oslo: Nasjonalt kunnskapssenter for helsetjenesten; 2015. Tilgjengelig fra: https://www.fhi.no/globalassets/dokumenterfiler/skjema/brukererfaring/2015_handbok_slik_oppsummerer_vi_forskning.pdf
- 28. da Silva PSL, Reis ME, Fonseca TSM, Fonseca MCM. Opioid and benzodiazepine withdrawal syndrome in PICU patients: which risk factors matter? J Addict Med. 2016;10(2):110–6. https://doi.org/10.1097/ADM.0000000000000197
- 29. Lang ES, Wyer PC, Haynes RB. Knowledge translation: closing the evidence-to-practice gap. Ann Emerg Med. 2007;49(3):355–63. https://doi.org/10.1016/j.annemergmed.2006.08.022
- 30. Brummel NE, Vasilevskis EE, Han JH, Boehm L, Pun BT, Ely EW. Implementing delirium screening in the intensive care unit: secrets to success. Crit Care Med. 2013;41(9):2196. https://doi.org/10.1097/CCM.0b013e31829a6f1e
- 31. Nielsen J. Usability 101: introduction to usability: world leaders in research-based user experience. Fremont: Nielsen Norman Group; 3. januar 2012. Tilgjengelig fra: https://www.nngroup.com/articles/usability-101-introduction-to-usability